REC: A Super-Pure Mesenchymal Stem Cell
超高純度MSCとしてのREC
PuRECが開発を進めている間葉系幹細胞は、ヒト骨髄液から抽出され、単に増える能力が高いだけでなく、骨や軟骨に分化する能力が極めて高いものが細胞1つのレベルで選別したものです。なんらかの遺伝子操作等を行うものではなく、ヒト骨髄液の候補細胞から性能の高いものを当社独自の技術で選別する形で得られます(「RECの製造方法」を参照)。すなわち、極めて純度の高い間葉系幹細胞です。早い段階で非常によく増えることから、「Rapidly(急速に) Expanding(増える) Clones(細胞株)」(略称REC)と名付けられています。
RECは、このほかに、動物実験において特に骨・軟骨に特に分化しやすい(分化能が高い)ことも確認されています。また、均一なサイズで、大きさも小さく、細胞内の硬い組織(細胞骨格)が未発達なため、からだの中を自由に駆け巡る能力(遊走能)が高いことも確認されています。

REC(製品・細胞)そのものの特性・優れている点
1.増殖能
一般的な間葉系幹細胞(MSC)は、骨髄中にごく少量しか含まれず、培養を重ねるうちに増殖能が低下し、細胞老化が進行することが知られています。
たとえば、骨髄由来のMSC集団には、分化・増殖能を備えた”真の幹細胞”は非常に少なく、1000細胞あたり1〜3個程度しか含まれていないとされています。
これに対してRECは、単一の細胞から1兆個(10¹²個)規模にまで増やすことが可能とされており、長期間にわたって高い増殖能を維持できる点が大きな違いです。
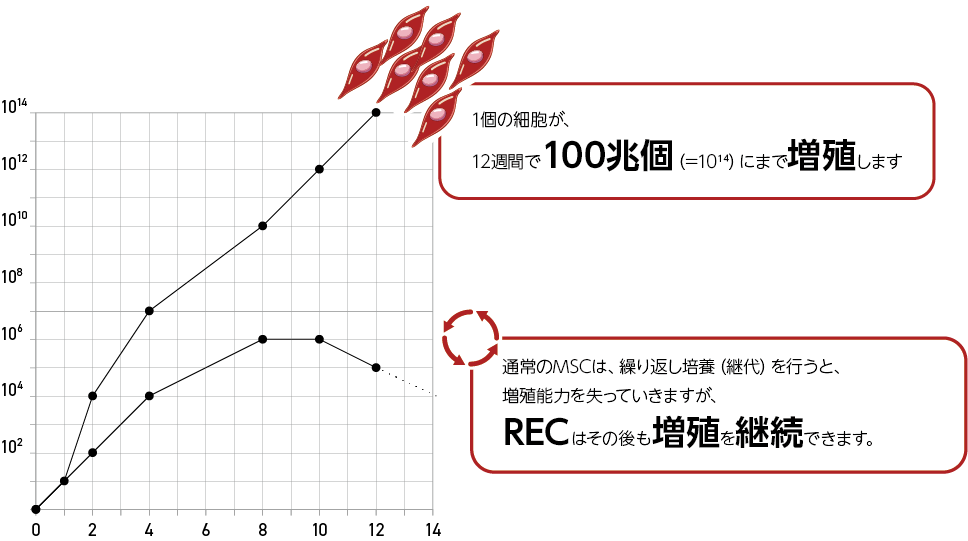
増殖能の高さの背景
RECの高い増殖性は、以下のような要素に支えられています。
1. 高増殖性クローンの選別
MSCには増殖スピードの異なるさまざまな細胞が混在しています。PuRECでは、最も増殖能力の高いクローン(細胞の起源となる単一の細胞)を選び出して培養しており、それが増殖の安定性につながっています。
2. 未分化性の維持
MSCは、未分化な状態から次第に分化(特定の機能を持つ細胞へ変化)していきます。RECは、MSCの中でも未分化な段階の細胞群を選別しているため、分化が進んだ細胞よりも増殖能力を保ちやすいと考えられています。
3. 他の細胞との影響を排除した単独培養
PuRECが行った実験では、RECを他の低増殖性細胞(SECなど)と混ぜて培養すると、REC単独で培養した場合に比べて全体の増殖効率が低下する結果が得られました。これは、周囲の細胞が出す因子が増殖に悪影響を与える可能性を示唆しています。そのため、RECを単独で培養することで、本来の増殖力を維持することができます。
幹細胞が高い増殖能を持つ場合、一般的に懸念されるのが「がん化」のリスクです。PuRECではこの点にも十分に配慮し、RECががん化していないことを、客観的かつ科学的に確認しています。 具体的には、「核型解析」と呼ばれる染色体レベルの検査を実施。これは、細胞に染色体異常(欠失・逆位・転座など)がないかを確認することで、がん化のリスクを評価する手法です。再生医療や細胞医薬品の分野では、ES細胞やiPS細胞を含む多くの細胞種でこの検査が推奨されており、細胞バンクの品質・安全性を担保するための標準的な評価方法とされています。 PuRECのRECもこの核型解析により、がん化の兆候となる染色体異常が検出されていないことが確認されています。これは、RECが単に増殖性に優れているだけでなく、治療応用において安全性の高い細胞であることを示す重要な根拠の一つです。
2.分化能
現在一般に利用されているMSCは純度の高い細胞以外に血球細胞や既に分化能が失われた細胞等の夾雑物の混入が避けられず、統一した幹細胞としての組織細胞への分化性能を持っていません。そのため、通常MSCを用いた治療においてはいわゆる「再生医療」においてイメージされる組織の再生等はあまり期待できず、ほとんどがMSCから分泌される物質の効能によってもたらされる「パラクライン・エフェクト」を期待した機序となっています。
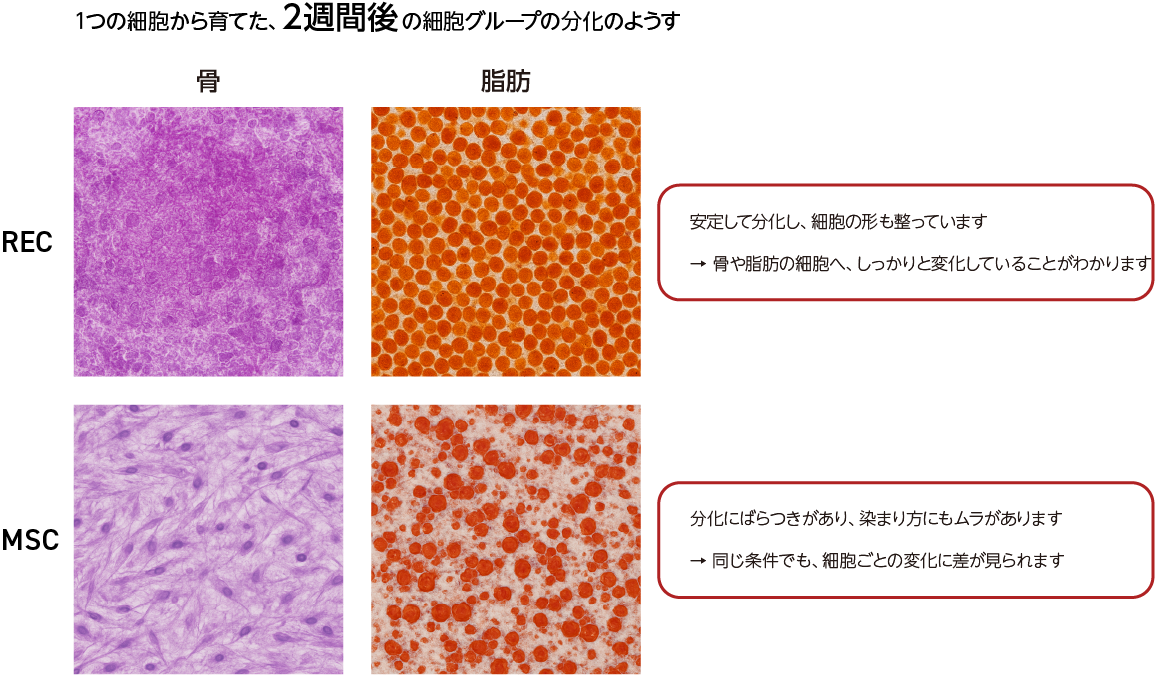
一方、当社のRECは非常に純度の高い高性能の細胞のみを選別して培養しているため、組織分化性能においても高い能力を持っています。下部のイメージ像にある通り、特に骨・軟骨の組織において非常に高い分化性能を持っているものであります。そのため、「再生医療」の本懐ともいえる組織再生の実現が可能となると考えており、臨床での応用を進めています。
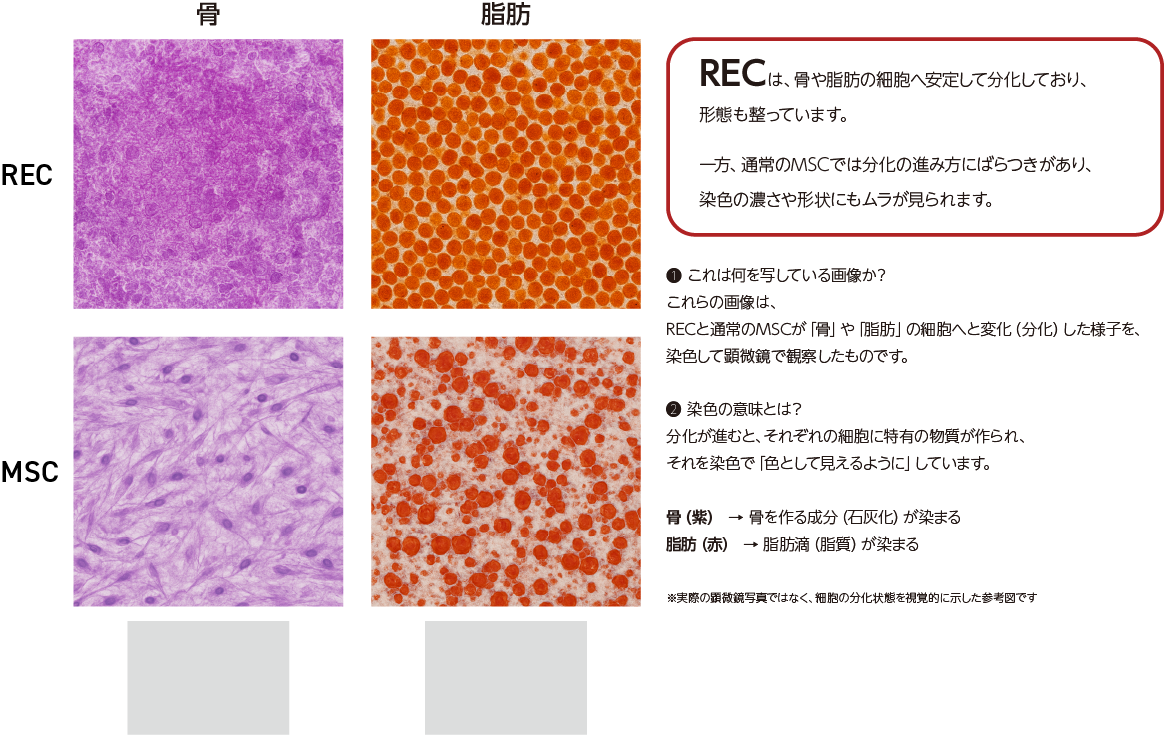
3.遊走能
細胞治療では、「届けたい場所に細胞がきちんと届き、そこで働くこと」が治療効果を得るための重要な前提です。
しかし、静脈を通して細胞を体内に投与する場合、最初に通過する肺の毛細血管で細胞が物理的に引っかかり、そこで止まってしまうことがあります。
特に、一般的に使用されているMSC(間葉系幹細胞)などの細胞加工物では、細胞のサイズが大きかったり、細胞同士が凝集しやすかったりする場合に、血管内で詰まる肺塞栓病を引き起こす可能性が指摘されています。
肺塞栓病は頻度こそ高くないものの、呼吸困難などを引き起こすリスクのある疾患であり、再生医療の現場でも重要な安全性上の懸念事項として慎重に扱われています。
実際に、細胞加工物を静脈内に投与する際には、細胞の凝集性や混入物(脂肪・組織片など)の管理、微小凝集塊を取り除くフィルターの使用など、あらかじめさまざまなリスク対策が講じられています。
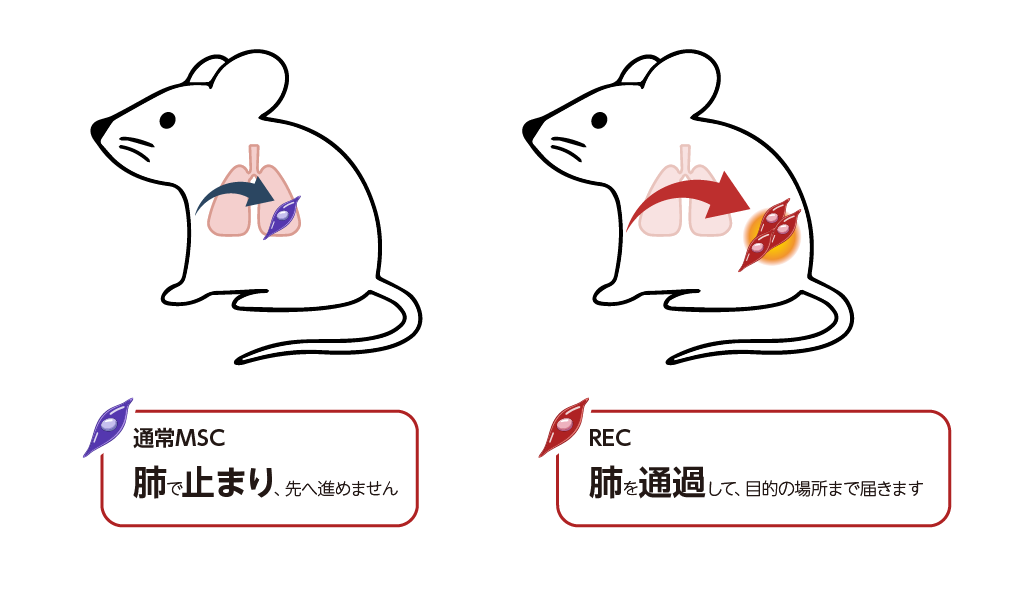
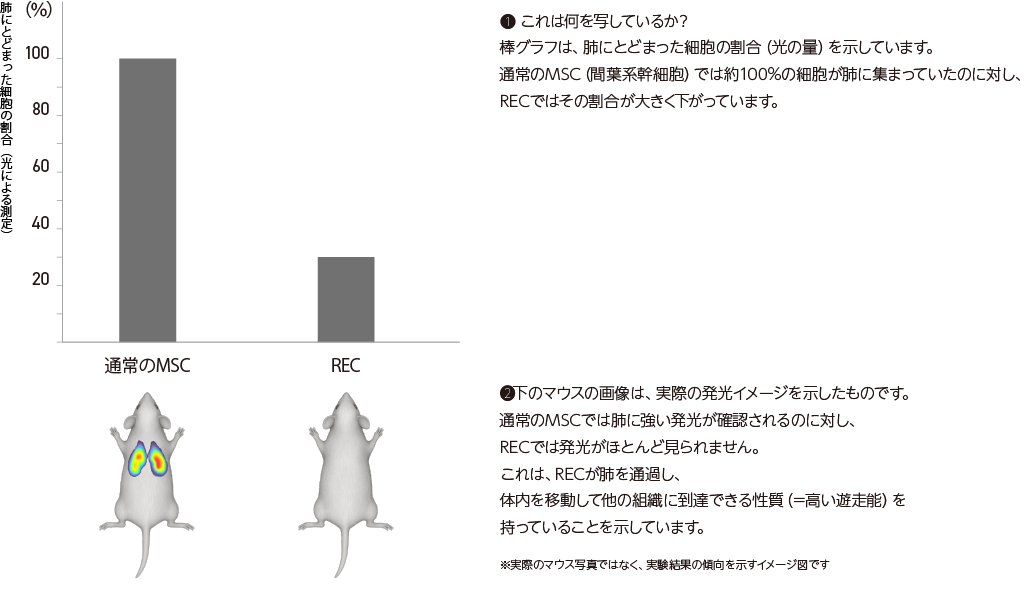
このような状況の中で、RECは「肺にとどまりにくい」細胞として、遊走能の高さが確認されています。細胞サイズが小さく、かつ均一であることにより、投与後に肺の毛細血管に引っかかることなく、目的の部位までしっかりと届くことが可能です。
上のイラストは、通常のMSCでは肺で細胞が滞留している一方、RECでは肺を通過し、目的の場所に移動している様子を示しています。
この画像は、細胞が体内でどこまで到達したかを観察するために行われた「蛍光染色」の結果です。
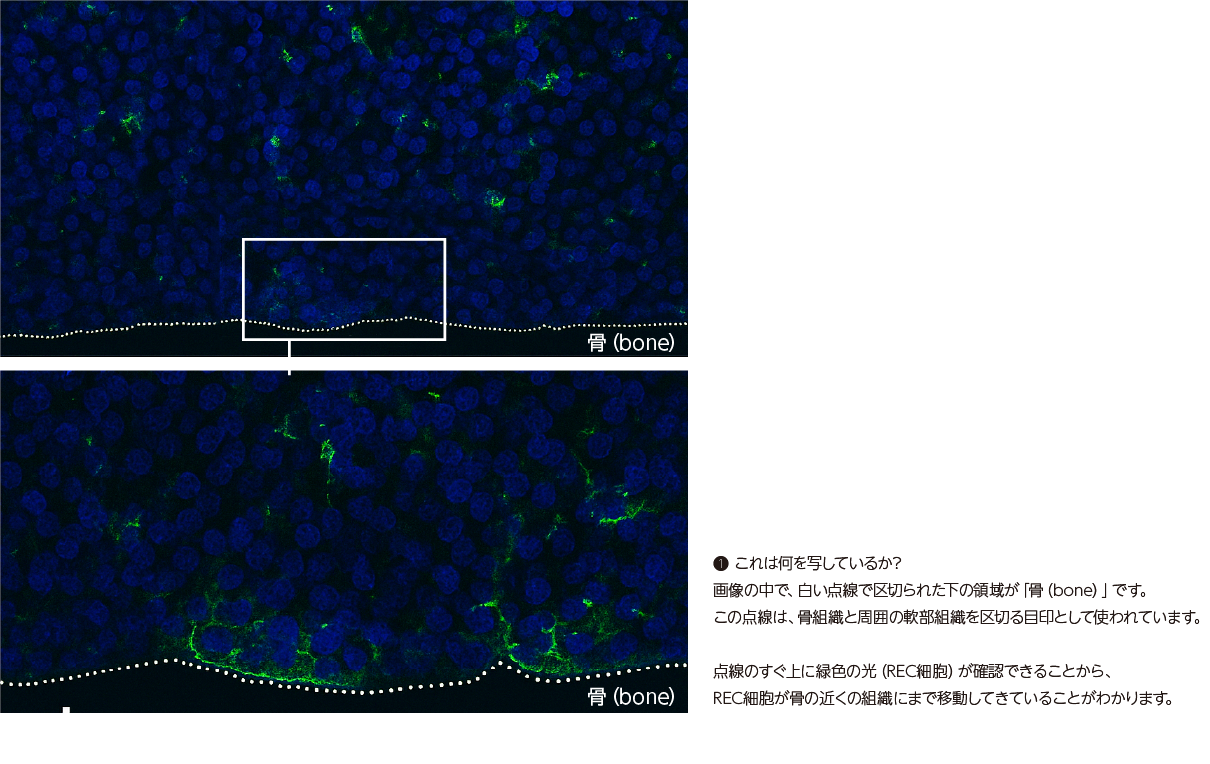
緑色に光っている部分(GFP)は、投与されたREC細胞の位置を示しています。
青は細胞の核を染めたもので、体内の組織構造を確認するための背景です。
注目すべきは、緑のREC細胞が、肺ではなく骨の近くにまで到達している点です。
これは、RECが血管を通って目的の場所に向かって移動する「遊走能」を実際に発揮していることを示しています。
このように、RECは「届けたい場所に届く」細胞として、治療の可能性を広げる力を持っていると考えられます。